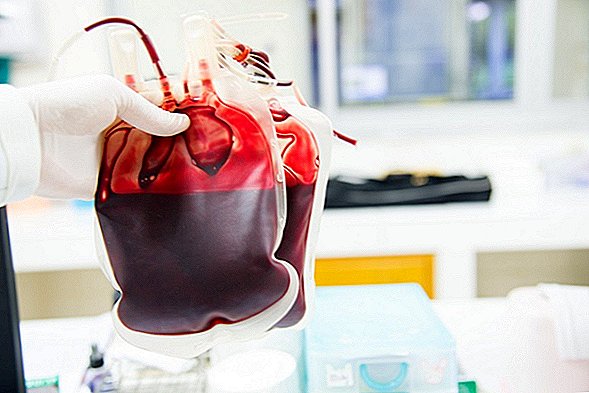
Si vous pensez que l'idée d'obtenir une transfusion de "sang jeune" pour prévenir le vieillissement semble farfelue, eh bien, les responsables de la santé américains sont d'accord.
Aujourd'hui (19 février), la Food and Drug Administration (FDA) des États-Unis s'est déclarée préoccupée par les informations faisant état de "mauvais acteurs" offrant des perfusions de plasma sanguin de jeunes pour traiter prétendument des affections et des maladies liées à l'âge, comme une perte de mémoire, Maladie de Parkinson et d'Alzheimer. Ces traitements sont non seulement non prouvés, mais ils comportent également des risques potentiellement graves, a déclaré l'agence.
"En termes simples, nous craignons que certains patients soient la proie d'acteurs sans scrupules vantant les traitements du plasma de jeunes donneurs comme des remèdes et des remèdes", ont déclaré le Dr Scott Gottlieb, commissaire de la FDA, et le Dr Peter Marks, directeur de la FDA. Center for Biologics Evaluation and Research, a déclaré dans un communiqué. "De tels traitements n'ont aucun avantage clinique prouvé pour les utilisations pour lesquelles ces cliniques les annoncent et sont potentiellement nocifs."
Le plasma est la partie liquide du sang et ne contient pas de cellules sanguines. Les transfusions de plasma peuvent sauver des vies pour les personnes qui subissent un traumatisme physique ou qui ont certaines maladies ou conditions qui empêchent leur sang de coaguler correctement.
Mais la FDA n'a pas approuvé les transfusions de plasma pour le traitement des affections et des maladies liées à l'âge, et ces traitements ne sont pas connus pour être sûrs ou efficaces.
"Nous décourageons fortement les consommateurs de poursuivre cette thérapie en dehors des essais cliniques" qui ont reçu un examen approprié et une surveillance réglementaire, ont déclaré Gottlieb et Marks.
De plus, certains rapports indiquent que ces transfusions non approuvées peuvent impliquer de grands volumes de plasma, et de telles doses importantes sont liées à des "risques importants", tels que des infections, des réactions allergiques et des problèmes respiratoires et cardiovasculaires, selon le communiqué.
La FDA a exhorté les consommateurs à consulter leurs médecins avant d'envisager de tels traitements. De plus, les essais cliniques qui testent des transfusions sanguines à des fins non encore approuvées par la FDA doivent avoir une "demande de nouveau médicament expérimental (IND)" avec la FDA, ce qui signifie que l'agence a examiné le traitement expérimental pour s'assurer qu'il est sûr . Donc, si la thérapie de transfusion sanguine est proposée dans le cadre d'un essai clinique, les gens devraient demander à voir le numéro IND et une copie de la communication de la FDA reconnaissant la demande, a indiqué l'agence.












